|
|
არასტეროიდული ანთების საწინააღმდეგო საშუალებები გიორგი გეგელაშვილი
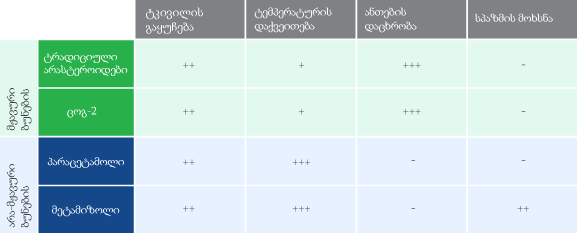
სინონიმები: Nonsteroidal anti-inflammatory drugs NSAIDs Nonsteroidal anti-inflammatory agents/analgesics NSAIAs Nonsteroidal anti-inflammatory medicines NSAIMs არასტეროიდები მჟავური ბუნების სხვადასხვა ქიმიურ სუბსტანციებს განეკუთვნებიან, მაგრამ მექანიზმი საერთოა - ამუხრუჭებენ ციკლოოქსიგენაზას - ცოგ და, შესაბამისად, აფერხებენ პროსტაგლანდინის სინთეზს. სწორედ პროსტაგლანდინის დათრგუნვაზეა დამყარებული არასტეროიდების ძირითადი ეფექტები: ტკივილგამაყუჩებელი ანალგეზიური ანთების საწინააღმდეგო ანტიფლოგისტური სიცხის დამწევი ანტიპირეტული. ცხრილი: ტკივილგამაყუჩებლების და არასტეროიდების შედარებითი ფარმაკოლოგია
ტერმინის ”არასტეროიდების” შემოღება განაპირობა ამ ჯგუფის პრეპარატების და კორტიკოსტეროიდების მომქმედების მექანიზმთან - ეიკოზანოიდების დათრგუნვასთან და, შესაბამისად, ძირითად ფარმაკოლოგიურ ეფექტთან - ანთების შემცირებასთან მსგავსებამ. არასტეროიდები მიეკუთვნება არაოპიოიდურ (არანარკოტიკულ) ტკივილგამაყუჩებლების ჯგუფს. ყველაზე გავრცელებული წარმომადგენლებია: ასპირინი, იბუპროფენი და ნაპროქსენი. ეს პრეპარატები რეგისტრირებულია პრაქტიკულად მსოფლიოს ყველა ქვეყანაში და ურეცეპტოდ გაიცემა. [1]
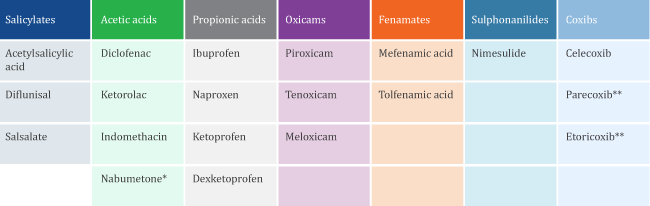
ტრადიციული (კლასიკური, ”არა-სელექციური”) არასტეროიდები დიდი ხანია მიმოქცევაშია მსოფლიოს ფარმაცევტულ ბაზარზე. იმთავითვე ამ პრეპარატებმა მნიშვნელოვანი ადგილი დაიკავეს ართრიტის და სხვა მტკივნეული ანთებითი მდგომარეობების დროს. ცოგ-ინჰიბიცია ზემოქმედებას ახდენს თრომბოქსანის და ლეიკოტრიენების სინთეზზე, რაც განაპირობებს პრეპარატების გვერდით მოქმედებას. ტრადიციული არასტეროიდებია სალიცილის მჟავას წარმოებულები - სალიცილატები ძმარმჟავას წარმოებულები პროპიონის მჟავას წარმოებულები - პროპიონატები ენოლის მჟავას წარმოებულები - ოქსიკამები ფენამის მჟავას წარმოებულები - ფენამატები სულფონანილიდები კოქსიბები შედარებით ახალი პრეპარატებია, რომლებიც უპირატესად თრგუნავენ ცოგ-2-ს და მათ ცოგ-2-სელექციურ ან ცოგ-2-სპეციფიურ არასტეროიდებს უწოდებენ. არასტეროიდების მოკლე კლასიფიკაცია
შენიშვნები: * – ნაბუმეტონი არ არის ძმრის მჟავას წარმოებული, მაგრამ მისი მთავარი მეტაბოლიტი შედის ამ ჯგუფში. ** – ძირითადად რეგისტრირებულია ევროკავშირის ქვეყნებში. როფეკოქსიბი, ვალდეკოქსიბი, ლუმირაკოქსიბი, ფიროკოქსიბი – შეუწყდათ რეგისტრაცია ან სამედიცინო მიზნით არ გამოიყენება.
არასტეროიდები განსაკუთრებით ეფექტურია იქ, სადაც ანთება და ტკივილი ერთდროულად თანაარსებობს. სიმპტომური მკურნალობის ძირითადი ჩვენებებია: [2] რევმატოიდული ართრიტი ოსტეოართრიტი ანთებითი ართროპათიები მაანკილოზებელი სპონდილიტი რეაქტიული ართრიტი (რეიტერის სინდრომი) ფსორიაზული ართრიტი ნიკრისის ქარის (პოდაგრის) შეტევა დისმენორეა (ალგომენორეა, მენზესური ტკივილი) ძვლის მეტასტაზური დაზიანება თავის ტკივილი (შაკიკი, დაზაბული ტიპის თავის ტკივილი და სხვ.) ოპერაციის შემდგომი ტკივილი ქსოვილების ანთებით ან ტრავმით განპირობებული სხვადასხვა სახის მსუბუქი და ზომიერი ტკივილი ცხელება (პირექსია) თირკმლის ჭვალი (კოლიკა) არტერიული (ბოტალოს) სადინრის შეუხორცებლობა ახალშობილებში. ასპირინის უნიკალური ეფექტი - ცოგ-1 შეუქცევადი დამუხრუჭება საფუძვლად უდევს თრომბოზის პრევენციას. ბოლო დროს ლიტერატურაში ბევრი იწერება არასტეროიდების კოლორექტული სიმსივნის პრევენციულ მოქმედებაზეც. საუკუნის დასაწყისში აშშ-ში რეცეპტით გამოიწერებოდა 70 მილიონი, ხოლო ურეცეპტოდ იყიდებოდა 30 მილიარდი სხვადასხვა არასტეროიდების კოლოფი (შეფუთვა) წელიწადში. [3]
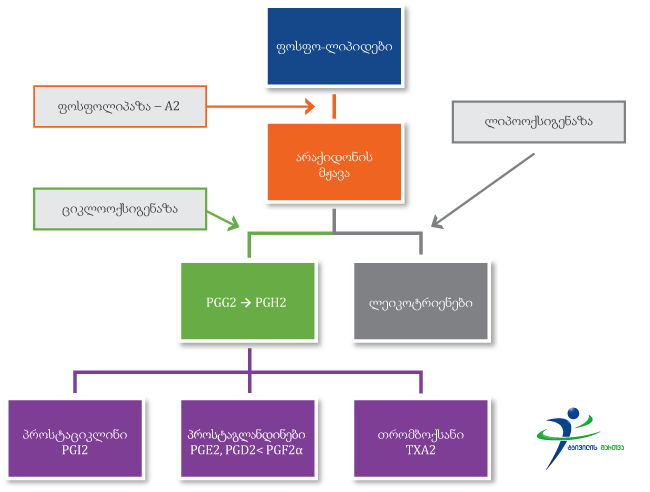
ანთების ან სხვადასხვა დაზიანების დროს ფოსფოლიპაზა-A2 ხელს უწყობს არაქიდონის მჟავას გამოათავისუფლებას უჯრედის მემბრანის ფოსფოლიპიდებისგან. არაქიდონის მჟავა ციკლოოქსიგენაზას (ცოგ) მეშვეობით გარდაიქმნება პროსტაგლანდინებად, პროსტაციკლინად და თრომბოქსანად, ხოლო ლიპოოქსიგენაზას მეშვეობით - ლეიკოტრიენებად. არასტეროიდები ამუხრუჭებენ ციკლოოქსიგენაზას აქტივობას და ამცირებენ უპირატესად პროსტაგლანდინების წარმოქმნას. ანთების საწინააღმდეგო ეფექტი არასტეროიდები ანთების ადგილზე ამცირებენ პროსტაგლანდინების კონცენტრაციას; რასაც თან ახლავს ბრადიკინინის, ენდოგენური პიროგენების, სხვა ბიოლოგიურად აქტიური ნივთიერებების, ჟანგბადის რადიკალების და NO-ს წარმოქმნის შემცირება. ტკივილგამაყუჩებელი ეფექტი ზ.ა მოქმედების შედეგად არასტეროიდები ამცირებენ ტკივილის რეცეფციას და, შესაბამისად, ამცირებენ ტკივილის აღქმას. სიცხის დამაქვეითებელი მოქმედება სხეულის ტემპერატურის მატებას განაპირობებს პროსტაგლანდინ-E2-ის მომატება ჰიპოთალამუსში. პროსტაგლანდინების კონცენტრაციის შემცირება, მათ შორის თავზურგტვინის სითხეში, იწვევს სხეულის ტემპერატურის ნორმალიზაციას.
არაქიდონის მჟავა უჯერი ცხიმოვანი მჟავაა და ძირითადად უჯრედის მემბრანის ფოსფოლიპიდებთანაა შეჭიდული. მას შემდეგ რაც, არაქიდონის მჟავა ფოსფოლიპაზა-A2 -ის მეშვეობით განთავისუფლდება ფოსფოლიპიდების ”კლანჭებიდან”, იწყებს ორი მიმართულებით გარდაქმნას: ციკოლოოქსიგენაზას (ცოგ-COX) მეშვეობით არაქიდონის მჟავა გარდაიქმნება პროსტაგლანდინებად და თრომბოქსანებად ლიპოოქსიგენაზას (ლოგ-LOX) მეშვეობით არაქიდონის მჟავა გარდაიქმნება ლეიკოტრიენებად.
ძირითადი პროსტაგლანდინებია PGE, PGF. მოანაწილეობენ ანთებით და სხვადასხვა პროცესებში. ყველაზე წარმოჩინებული ანთებითი პროსტაგლანდინია PGE2. იგი აფართოებს სისხლძარღვებს, ზრდის მათ განვლადობას, აძლიერებს ჰისტამინის და ბრადიკინის აქტივობას, იწვევს ცხელებას. პროსტაგლანდინები ამცირებენ ნოციცეპტორების ტკივილის ზღურბლს. PGE1,2 და PGI2 იცავენ კუჭის და ნაწლავების ლორწოვანს. პროსტაგლანდინები ხელს უწყობენნ რენინის პროდუქციას თირკმელში და საშვილოსნოს შეკუმშვას.
თრომბოქსანი A2 ხელს უწყობს თრომბოციტების აგრეგაციას და ამგვარად მონაწილეობს სისხლის შედედების პროცესში.
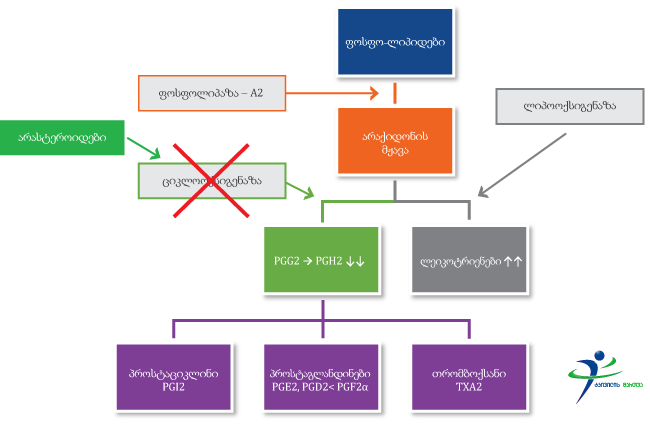
არასტეროიდები, თრგუნავენ რა ციკლოოქსიგენაზებს, აფერხებენ პროსტაგლანდინების და თრომბოქსანის სინთეზს და ”გზას უხსნიან ” არაქიდონის მჟავადან ლეიკოტრიენების წარმოშობას. ლეიკოტრინები სუსტი ანთებითი და ძლიერი ალერგიული მედიაქტორებია.
[1]
Warden, Stuart J. "Prophylactic Use of NSAIDs by Athletes: A Risk/Benefit Assessment".The Physician and Sports Medicine. April 2010. 38 (1): 132–138.
1. Allgemeine und spezielle Pharmakologie und Toxikologie, Für Studenten der Medizin, Veterinärmedizin, Pharmazie, Chemie und Biologie sowie für Ärzte, Tierärzte und Apotheker. 9th ed. München: Elsevier, Urban & Fischer, 2005. xxvi, 1189. ISBN: 9783437425219. Available from: www.worldcat.org/oclc/56878844.2. Edwards JE, Oldman AD, Smith LA, et al. Oral aspirin in postoperative pain: a quantitative systematic review. Pain 1999;81:289–97. 3. Gao R, Li X. Risk assessment and aspirin use in Asian and Western populations. Vasc Health Risk Manag 2010;6:943–56. 4. Hawkey CJ. Review article: aspirin and gastrointestinal bleeding. Aliment Pharmacol Ther 1994;8:141–6. 5. Jenkins C, Costello J, Hodge L. Systematic review of prevalence of aspirin induced asthma and its implications for clinical practice. BMJ 2004;328:434. 6. Skoutakis VA, Carter CA, Mickle TR, et al. Review of diclofenac and evaluation of its place in therapy as a nonsteroidal antiinflammatory agent. Drug Intell Clin Pharm 1988;22:850–9. 7. Beaver WT. Review of the analgesic efficacy of ibuprofen. Int J Clin Pract Suppl 2003;(135):13–7. 8. Southey ER, Soares-Weiser K, Kleijnen J. Systematic review and meta-analysis of the clinical safety and tolerability of ibuprofen compared with paracetamol in paediatric pain and fever. Curr Med Res Opin 2009;25:2207–22. 9. Cooper SA. Review of ketoprofen. J Clin Dent 1988;1:1–5. 10. Schoenfeld P. Gastrointestinal safety profile of meloxicam: a meta-analysis and systematic review of randomized controlled trials. Am J Med 1999;107:48S-54S. 11. Mason L, Edwards JE, Moore RA, McQuay HJ. Single-dose oral naproxen for acute postoperative pain: a quantitative systematic review. BMC Anesthesiol 2003;3:4. 12. Ward A, Brogden RN. Nimesulide. A preliminary review of its pharmacological properties and therapeutic efficacy in inflammation and pain states. Drugs 1988;36:732–53. 13. Page M, Christin F, Hayi-Slayman D, et al. [Acute liver failure due to a treatment by nimesulide: another case and review], Hepatite fulminante liee a un traitement par nimesulide: encore un cas et revue de la litterature. Ann Fr Anesth Reanim 2008;27:742–6. 14. Ando GA, Lombardino JG. Piroxicam–a literature review of new results from laboratory and clinical studies. Eur J Rheumatol Inflamm 1983;6:3–23. 15. Chen YF, Jobanputra P, Barton P, et al. Cyclooxygenase-2 selective non-steroidal antiinflammatory drugs (etodolac, meloxicam, celecoxib, rofecoxib, etoricoxib, valdecoxib and lumiracoxib) for osteoarthritis and rheumatoid arthritis: a systematic review and economic evaluation. Health Technol Assess 2008;12:1-278, iii. 16. Mateos JL. [Selective inhibitors of cyclooxygenase-2 (COX-2), celecoxib and parecoxib: a systematic review], Inhibidores selectivos de la ciclooxigenasa-2 (COX-2), celecoxib y parecoxib: una revision sistematica. Drugs Today (Barc) 2010;46 Suppl A:1–25. 17. Aldington S, Shirtcliffe P, Weatherall M, Beasley R. Systematic review and meta-analysis of the risk of major cardiovascular events with etoricoxib therapy. N Z Med J 2005;118:U1684. 18. Croom KF, Siddiqui MA. Etoricoxib: a review of its use in the symptomatic treatment of osteoarthritis, rheumatoid arthritis, ankylosing spondylitis and acute gouty arthritis. Drugs 2009;69:1513–32. 19. Hackenthal E. Paracetamol und Metamizol in der Therapie chronischer Schmerzen. Ubersicht uber klinische Studien. Schmerz 1997;11:269–75. 20. Morgan O, Majeed A. Restricting paracetamol in the United Kingdom to reduce poisoning: a systematic review. J Public Health (Oxf) 2005;27:12–8. 21. Macario A, Royal MA. A Literature Review of Randomized Clinical Trials of Intravenous Acetaminophen (Paracetamol) for Acute Postoperative Pain. Pain Practice 2010. 22. Rohdewald P, Neddermann E. Dosisabhangigkeit der analgetischen Wirkung von Metamizol. Anaesthesist 1988;37:150–5. 23. Ibanez L, Vidal X, Ballarin E, Laporte JR. Agranulocytosis associated with dipyrone (metamizol). Eur J Clin Pharmacol 2005;60:821–9. 24. Friedel HA, Fitton A. Flupirtine. A review of its pharmacological properties, and therapeutic efficacy in pain states. Drugs 1993;45:548–69. Warden, Stuart J. "Prophylactic Use of NSAIDs by Athletes: A Risk/Benefit Assessment".The Physician and Sports Medicine. April 2010. 38 (1): 132–138. Simone Rossi, ed. (2006). Australian medicines handbook 2006. Adelaide: Australian Medicines Handbook Pty Ltd. Green, Ga. "Understanding NSAIDs: from aspirin to COX-2". Clinical cornerstone. 2001, 3 (5): 50–60. |
|
|
|||||||||||||||||||||||||||||||||||||||||